佳维斯(武汉)生物医药有限公司
3 年
手机商铺
- NaN
- 0.9000000000000004
- 0.9000000000000004
- 1.9000000000000004
- 0.9000000000000004
推荐产品
公司新闻/正文
Nature | 组织透明化三维成像揭示AD发病重要因素
98 人阅读发布时间:2025-09-10 16:45
阿尔茨海默病(Alzheimer's Disease, AD)是一种神经退行性疾病,通常表现为记忆力减退、认知能力下降和其他智力功能障碍,导致痴呆的主要原因之一,其发病率随着年龄增长迅速上升,但为什么年龄是主要风险因素仍不清楚。近期来自德国的马克斯·普朗克多学科研究所的Klaus-Armin Nave团队在Nature上发表题为”Myelin dysfunction drives amyloid-β deposition in models of Alzheimer’s disease”的文章或揭示年龄增长导致阿尔兹海默病患病率增高的具体机制。

在中枢神经系统中,神经元轴突为了维持高速的动作电位传递,需要借助髓鞘将其包裹,似于电线的绝缘皮,而少突胶质细胞负责髓鞘的产生。长期以来,人们一直认为AD的主要病因是淀粉样斑块(Amyloid Plaques)和Tau蛋白的异常聚集,导致神经元的损害和死亡。因此,大多数治疗策略都针对这两个蛋白进行研究,髓鞘脱失经常被视为AD病理发生后的下游产物。但由于代谢更新缓慢,随着人体的衰老,髓鞘极可能是生理状态下在CNS中比较早出现缺陷的结构。作者认为,当髓鞘受损时,会触发一系列事件,包括微胶质细胞(Microglia)的激活、轴突的损伤和淀粉样斑块的形成。根据AD的淀粉样假说,Aβ的积累引发了一系列有害事件,最终导致神经元功能障碍。由于少突胶质细胞支持轴突能量代谢和神经细胞健康,因此失去髓鞘完整性可能是导致神经淀粉样蛋白(Aβ)沉积的上游风险因素。而髓鞘功能障碍导致Aβ生成机制在轴突肿胀内积累,并增加了皮层淀粉样前体蛋白的切割。尽管总体上微胶质细胞数量增加,但具有髓鞘功能障碍的AD小鼠缺乏通常清除淀粉样斑块的微胶质细胞。
为了验证髓鞘损伤的确能够推进淀粉样沉积这一AD重要病理。研究团队首先培育了髓鞘功能损伤的Cnp−/−和Plp−/y小鼠模型,然后将它们与常用的AD小鼠模型进行交叉繁殖。随后作者运用iDISCO组织透明技术,分析Cnp−/−和Plp−/y小鼠与5×FAD小鼠的后代以及APPNLGF knock-in小鼠模型,这两种AD病例背景下所产生淀粉样蛋白沉积的变化,并运用光片显微镜进行测量,这种方法可以直观且无偏差地测量整个大脑中淀粉样斑块的分布和数量。
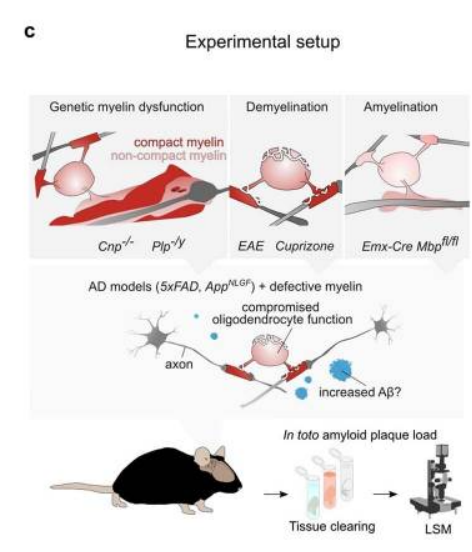
图1研究髓磷脂功能障碍对AD小鼠模型中淀粉样斑块负荷影响的实验设计
研究结果表明,髓鞘损伤小鼠在6个月龄时显示出明显增加的淀粉样斑块负荷,其在海马白质和皮质中的增加尤为显著。而未发现6个月龄的5×FAD小鼠或APPNLGF小鼠存在明显的髓鞘病理变化,这表明观察到的效应不是髓鞘对淀粉样斑块的次生反应。并且,文章还在5×FAD背景下使用了EAE和cuprizone两种急性脱髓鞘模型,证明淀粉样蛋白车技在脱髓鞘病灶内的数量增高。研究结果表明髓鞘缺陷可能是淀粉样斑块沉积的上游驱动因素。这些结果对于理解阿尔茨海默病的病理机制具有重要意义。
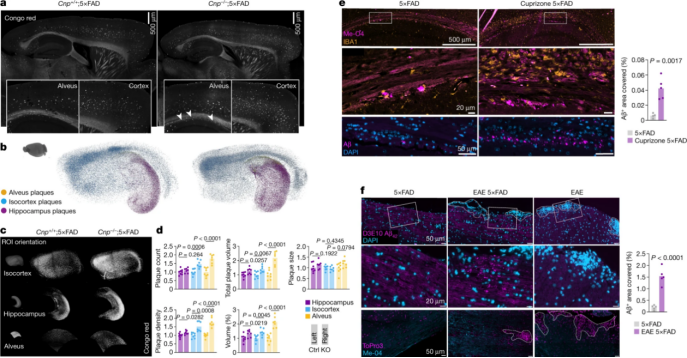
图2 髓鞘形成和脱髓鞘增强5×FAD小鼠的淀粉样斑块沉积
文章后续还采用了行为学、RNA测序及单细胞测序等一系列实验方法,验证少突胶质细胞与髓鞘缺失在AD致病过程中的重要作用,促进髓鞘健康应被视为延缓或预防AD的治疗目标。而组织透明及光片技术,可以对AD的病理产物的观察更容易可视化和分析,使实验结果更为完整直观。